信頼性保証体制 
信頼性保証体制 
社長直轄の独立部門が、信頼性保証に対する現場支援と監査およびPL*・品質保証アセスメントを担当しています。また、市販後調査等の実施および副作用情報や品質情報などの収集・管理により、製造販売後の信頼性保証を担っています。*PL:Product Liability(製造物責任)
帝人グループのPL・品質保証アセスメント制度を研究開発の管理に運用
帝人ファーマでは、法規や公的基準の遵守はもとより、さらに厳しい社内規定を導入。
研究開発管理規定のなかには、帝人グループのPL・品質保証アセスメント制度を組み込み、信頼性保証のシステムとして機能させています。
また、技術・設計面から人事・組織管理、営業、物流までを信頼性保証の適応範囲に含み、アセスメントを実施しています。
副作用情報はグローバルに収集しデータベース化
帝人ファーマでは、薬事法に則り、医療機関や国内・海外の提携先および公表論文等から副作用情報を収集。
集められた情報は担当部署に集約され、世界の主要提携企業とも情報共有できるようデータベース化し、
安全性情報の解析や副作用情報の発信に役立てています。
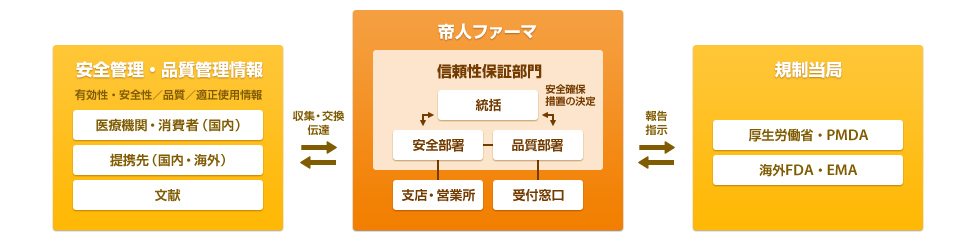
医薬品と医療機器に関する信頼性保証のための安全管理・品質管理体制(市販後)
-
FDA: Food and Drug Administration(アメリカ食品医薬品局)
-
EMA: European Medicines Agency(欧州医薬品審査庁)
-
PMDA: Pharmaceuticals and Medical Devices Agency(医薬品医療機器総合機構)
世界展開に合わせ、
信頼性保証もグローバル対応へ
いままで欧米中心だった提携先は、「フェブリク」のグローバル展開を発端として、世界各国に広がっています。海外のリスク構造は国内同様、法令リスク、品質リスク、安全リスクが中心となりますが、その中身は国や地域で異なり、リスク管理やその対応にはそれぞれのノウハウが必要となります。
海外リスク管理において重要なのは、品質と安全の保証を確実に実施できる企業と提携すること。そして、リスク管理が確実に実施されているか、継続的に確認する体制を構築することです。前述のPLアセスメントにおいても海外パートナーのリスク管理能力、リスク対応能力のチェックが重要な要素となっています。グローバル展開に合わせ、帝人ファーマはグローバルな信頼性保証の体制づくりに取り組んでいます。
医療現場に貢献する包括的なサービス:「顧客・マーケット対応」